クロフィブラートなどPPARリガンド(アゴニスト)の作用機序のまとめ
クロフィブラートなどPPARリガンド(アゴニスト)が、どのようにして皮膚炎を抑えるのか?現時点(2012年9月)でわかっているメカニズムをまとめてみます。
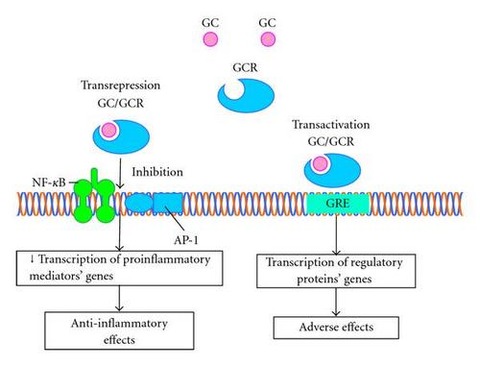
まず、ステロイドがどのようにして炎症を抑えるのか?のおさらいです。GC(ピンクの丸)がステロイドでGCRがステロイドレセプターです。ステロイドがレセプターに結合して活性化すると、DNAに対して二つの働きをします。一つは左側、NF-κBによって産生される炎症メディエーターを抑える働きです(現在開発中のNF-κBデコイも同じくこの個所で働きます)。
もう一つは右側に示されているように、GC/GCR結合体が直接DNAに働いて何かの物質の転写を促す働きです。
(図はTargeting Nuclear Hormone Receptors: PPARα Agonists as Potential Disease-Modifying Drugs for Rheumatoid Arthritis, I V. Shirinsky et al, International Journal of RheumatologyVolume 2011 (2011) からお借りしました)

PPARリガンドはPPARに結合して、GC/GCR同様、NF-κBを抑制する働きをします。したがって、ステロイドやNF-κBと同様、抗炎症作用を持ちます。その一方でGC/GCRのDNAへの直接作用の抑制にも働きます。ステロイドの副作用(Adverse effects)は、この直接作用によって生じます(もっとも、ここで言う「ステロイドの副作用」とは、「抗炎症作用でないその他の作用」というべきもので、必ずしも依存性に関係した副作用のことではなく、もっと一般的な副作用のことです)。
「ステロイドとPPARリガンドとは、作用する個所がNF-κBの抑制という同じ個所であるならば、両者はどこが違うのか?PPARリガンドもステロイドと同じようにリバウンドを起こすのではないか?」と疑問を抱くかもしれません。どこが違うかというと、組織や臓器、各細胞における、PPARの分布が、ステロイドレセプターの分布とは大きく違う、この点が大きいと私は考えます。
ステロイドを内服すれば、リンパ球などの免疫系が強く抑えられます。これは、リンパ球がステロイドレセプターを豊富に持っているからです。一方、PPARリガンドであるクロフィブラートを内服しても、強い免疫抑制は起きません。たぶん(調べても明記した文献が見つからないので私の推測ですが)リンパ球にはPPARが発達していないからだと考えられます。
さらに、PPARには、αβγの3種類があります。これらの分布もまた異なるようです。たとえば、マクロファージやランゲルハンス細胞など、抗原提示機能のある樹枝状細胞にはPPARγが多いです。
一方、表皮細胞は、TSLPという炎症性メディエーターを産生して、アトピー性皮膚炎の慢性化(ペリオスチン経路の悪循環)の一環を担っていますが、この表皮細胞のTSLP産生は、PPARαアゴニストで抑制されるようです(注)。
ですから、単純化すると、PPARαリガンド(クロフィブラート)は表皮細胞のTSLPを抑え、PPARγリガンド(AVANDIA)は表皮のランゲルハンス細胞を抑制する、と言えます。
以前、佐賀大の論文中の下図を引用して、解説しましたが、

PPARリガンドというのは、赤丸の中、表皮細胞のTSLP産生のところ、あるいは、APCs(樹枝状細胞)の機能、その辺りにのみ、効果をもたらすわけです。
ステロイドの場合は、この悪化サイクルの、ほとんど全部のパーツを抑制します。抑制が多くの個所でかかりすぎて、どこかで部分的にpositive feedbackのようなことが生じていて、中止すると、はずみでこのサイクルが回りだしてしまう、これがリバウンドではないか?というのが私の仮説です(→こちら)。
ですから、このvicious circleを、どこかある個所でだけ、とめてやると、リバウンドは早く収束するのではないか?と考えたわけです。

Viciouc circleというのは、糸車のようなものとイメージすると解りやすいかもです。最初にアトピー性皮膚炎で炎症が生じて、これをステロイドで抑えてやると、カラカラと回っていた糸車は、ぴたっと止まりますが、その一方で「糸車を回そう」という力も加わっていると考えられます。ステロイドには、糸車を止めようとする力と、回そうとする力とがあり、止めようとする力>回そうとする力、なので、外用中は糸車は止まっている、ということです。ほかに、中止後リバウンドが生じるメカニズムが考えられません。
ステロイドを中止すると、たぶん、止めようとする力が消えるよりも、回そうとする力が消えるほうが、少しだけ遅れるのでしょう(複数の経路を介したメカニズムであるためではないかと考えます。以前「リバウンドとは時差(time lag)である」と表現しました)、糸車は勢いよく回り始めます。自然に収束するのを待つしかありません。これがリバウンドです。
PPARの作用というのは、このサイクルの一部分にしか作用しないため、弱いですが、投与すれば糸車を確実に抑えてくれるものだと考えます。リバウンドを起こしません。繰り返し記しますが、およそ薬剤で、ステロイド外用剤のような「リバウンド現象」を来たすものを、私はほかに知りません。非常に珍しい現象です。(1)ステロイドの作用が非常に広範にわたり、しかも(2)皮膚(表皮細胞)を介するvicious circle(輪が閉じている)が形成されているため、たまたま成立した現象だと解します。
PPARαの外用が無効でも、PPARγの外用なら効く可能性がある、と私が考えたのも、上記からご理解いただけると思います。ターゲットがそれぞれ表皮細胞とランゲルハンス細胞であり違うのです。どちらもVicious circleの一部分である点は同じです。
「PPARリガンドならは、EPAやDHAという、天然由来のものもありますが、なぜクロフィブラートを選ばれたのですか?」というご質問を受けました。また、先日、練馬区の皮膚科開業医である藤澤先生からも電話で「(PPARリガンドなら)エパデール(EPAの製剤)でいいんだろ?」と尋ねられました。私が、エパデールではなく、クロフィブラートを選んだ理由は三つあります。
1) EPAやDHAは臭いがあり(魚の臭い)二重盲験が成立しない
2) 動物実験で用いられているのは、クロフィブラートなど、合成PPARリガンドであり、EPAやDHAについてのデータは文献が見つからない。
3) おそらく、抗脂血症の薬剤としての臨床効果からの推測として、天然由来のPPARリガンドであるEPA、DHAの効果は、クロフィブラートよりも弱い。
です。
一方、EPAやDHAを用いた軟膏についてのデータが無いかと調べたら、ありました。
The effect of a newly developed ointment containing eicosapentaenoic acid and docosahexaenoic acid in the treatment of atopic dermatitis
T Watanabe et al
The Journal of Medical Investigation Vol.46 1999 173-177
です。
高松市民病院小児科の渡辺俊之先生というかたの、1999年の報告で、おそらく臭いのためでしょう、二重盲験ではなく、実薬とコントロールとの左右塗りわけによって、小児アトピー性皮膚炎における改善効果を確認しています。
この頃は、まだPPARのメカニズムが知られていなかったため、考察に言及はありませんが、今考えてみると、これは、EPA,DHAがPPARリガンドであることによる効果とも解されます。

渡辺先生の臨床研究は、ダイアフラジン軟膏という一般薬という形で反映されたようで、ネットで検索してみると、結構、このダイアフラジン軟膏を用いて脱ステロイドのリバウンドの抑えに有効であった、といった患者たちの体験談が出てきます。
比較をしていないので断言は出来ませんが、ダイアフラジン軟膏で効くならば、クロフィブラートやAVANDIAの軟膏ならば、さらに効果は強いと推測します。ちょうど、ステロイドでも、強さのランクがあって、生理的なコーチゾンよりも、合成ステロイドのほうが効果が高いのと同じようにです。
PPARリガンドには、この他にも非常に多くの物質がありますから、将来的には、どのようなPPARリガンドが、アトピー性皮膚炎やリバウンドの外用薬として最適なのか、あるいは、どのような病態の時には、どのPPARリガンドが有効なのか、といったデータベースが蓄積されていくと良いと思います。
注)ケラチノサイトは、クロフィブラートなどのPPARαに反応します(Organotypic Modeling of Human Keratinocyte Response to Peroxisome Proliferators., Zhang C et al. Cells Tissues Organs. 2012 Jun 5)。また、TSLPの産生はNFκBによります(Inhibition of NFκB-Mediated TSLP Expression by Retinoid X Receptor. HC Lee et al. J Immunol. 2008 October 15; 181(8): 5189–5193)。この2つから、表皮細胞にはPPARαがあり、PPARαリガンドはNFκBを介してTSLP産生を抑制することが推測されます。
moto_tclinic at 23:50│Comments(0)│TrackBack(0)│
