ステロイド依存の分子生物学的メカニズムを考える(1)

KLK(カリクレイン)ファミリーの酵素遺伝子は、下記論文で示されているように、ステロイドの制御を受けやすいことが知られていたからです、
The KLK7 (PRSS6) gene, encoding for the stratum corneum chymotryptic enzyme is a new member of the human kallikrein gene family — genomic characterization, mapping, tissue expression and hormonal regulation |
この点についてのDr.Corkの指摘は、外れていたかもしれません。なぜなら、
| Kallikrein Expression and Cathelicidin Processing Are Independently Controlled in Keratinocytes by Calcium, Vitamin D3, and Retinoic Acid Shin Morizane et al. Journal of Investigative Dermatology (2010) 130, 1297–1306 |
によって、ヒトの表皮細胞に対して、さまざまなホルモンやビタミン、細胞増殖因子などを添加して、KLK7および5の発現を調べた実験結果が報告され、dexamethasoneすなわち副腎皮質ホルモンは、表皮細胞のこれら酵素の産生制御に関わっていないようだ、ということが示されたからです(ビタミンD、レチノイン酸、Caイオンなどによって、これら酵素の発現は制御されていました)。

しかし、Dr.Corkの表皮バリア破壊(epidermal barrier dysfunction)説で重要な点は、プロテアーゼに着目したことにあるのではありません。2006年に発表された彼の論文を読み返してみると、
| Topical corticosteroids are an important short-term treatment for severe flares of AD. However, if topical corticosteroids are used for prolonged periods and particularly on delicate skin sites, they can cause cutaneous atrophy and damage the stratum corneum. Prolonged use of topical corticosteroids might damage the skin barrier on delicate skin sites enough to enhance the penetration of irritants and allergens. This could provide the explanation for the phenomenon of posttopical steroid rebound and steroid addiction. (ステロイド外用剤はアトピー性皮膚炎の悪化の短期的な治療薬としては重要である。しかし、長期間、とくに感受性の強い部位に外用すると、角層を破壊し、表皮の萎縮をきたす。ステロイド外用剤の長期連用は敏感な部位での皮膚バリア破壊を介して、外的刺激やアレルゲンの侵入を引き起こす。このことは「ステロイド依存」と呼ばれるステロイド外用後のリバウンド現象の説明になる。) |
と記されています。
プロテアーゼというピンポイントでの指摘は外したかもしれませんが、ステロイド依存のメカニズムとして、表皮バリアの破壊を指摘したのは、Dr.Corkが初めてです。これは十分に大きな功績です。気管支喘息など、粘膜へのステロイド噴霧では、ステロイド依存の報告が見当たらない点などを、よく説明できるからです。
また、Dr.Morizaneらの論文は、表皮細胞への、直接の制御を調べたものですが、ステロイドホルモンが、間接的にKLK7や5の制御に関与することによってステロイド依存が生じている可能性は依然あります。その根拠は、
| Human tissue kallikrein expression in the stratum corneum and serum of atopic dermatitis patients Komatsu N et al. Experimental Dermatology Volume 16 Issue 6 , (June 2007) |
ステロイド外用剤により皮疹が良好にコントロールされているアトピー性皮膚炎患者のプロテアーゼを色々調べたところ、健常者対照に比べて、角層中のプロテアーゼ量が増加していたことなどが報告されています。
実験の概要ですが、まず患者および健常者の角質を一人あたり2mg集めるところから始まります。皮膚に粘着テープを貼ってはがすと、ここに角質が付いてきますので、これを一人当たり総量2mgになるまで繰り返します。
患者のプロファイルですが、14名(女9、男5)平均年齢27.4才で、アトピー性皮膚炎と診断されステロイド外用剤によって良好にコントロールされている患者の、乾燥肌(軽度苔癬化はあってもよい)から採取、とあります。
| The SC samples for AD were obtained from the forearms of 14 patients [nine females and five males, 27.4 ± 4.2 years old (mean ± standard deviation (SD))] who had been diagnosed with AD and were under medication with corticosteroid topical agents. All patients who provided the SC samples were well-controlled by the medication. The SC samples were collected only from dry skin with or without very mild lichenification, and joint areas were excluded. For consistency, the patients who showed moderate to strong lichenification, excoriation, crust, apparent scratch mark and secondary skin infection were excluded. |
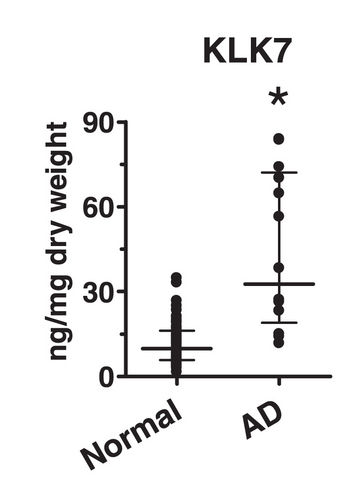
患者角層中のKLK7は、特異抗体を用いたELISA法による定量で、健常人よりも有意に増加していました。一方、血液中のKLK7量も同様に測定されていますが、こちらは差はありませんでした。したがって患者の皮膚局所のみにおけるプロテアーゼの増加が確認されたことになります。
プロテアーゼは酵素ですから、量の測定のほかに活性の測定もできます。KLK7はキモトリプシン様活性を持ちますから、適当な基質を使って、患者角質サンプル中のキモトリプシン活性を測ることで、KLK7活性に代用できると考えられました。その結果ですが、健常者サンプルと差がありませんでした。量では明らかな差があったのにです。
量と活性とのギャップはインヒビターによって説明可能です。KLK7にはLEKTI( Lympho-epithelial Kazal-type-related inhibitor)というインヒビターがあり、別のプロテアーゼ(フリン様活性をもつ)によって活性化されます。そこで、患者サンプル中のフリン活性を調べてみたところ、健常者に比して活性が有意に高いことがわかりました。

ステロイド外用剤でコントロールされた患者皮膚においては、KLK7が量的に増加しているが、その活性抑えられていて、その抑制は、別のプロテアーゼを介したインヒビターの活性化によって行われている、ということになります。
すなわち、「ステロイド外用剤で良くコントロールされた」アトピー性皮膚炎患者の皮膚では、実はKLK7が量的にup-regulateされており、これをインヒビターで抑えることで、なんとかコルネオデスモゾームが破壊されずに皮膚の構造が保たれている、という非常に危うい均衡の上にあると解釈できます。
これがステロイド外用による間接的な結果であって、中止によるリバウンドは、この均衡が崩れた(インヒビター<プロテアーゼとなった)ためだという可能性はあります。
ステロイド外用剤が、連用により、表皮バリアを破壊すること自体は、組織学的(→こちら)および生理学的(→こちら)に確認された事実です。しかし分子生物学的なメカニズムはまだ解明されていません。それはステロイドホルモンの表皮細胞への直接の作用によるのかもしれませんし、間接的な作用によるのかもしれません。(→こちらに続く)。
